Les scientifiques ont, pour la première fois, libéré avec succès des embryons d’un gène défectueux qui provoque une maladie cardiaque génétique.
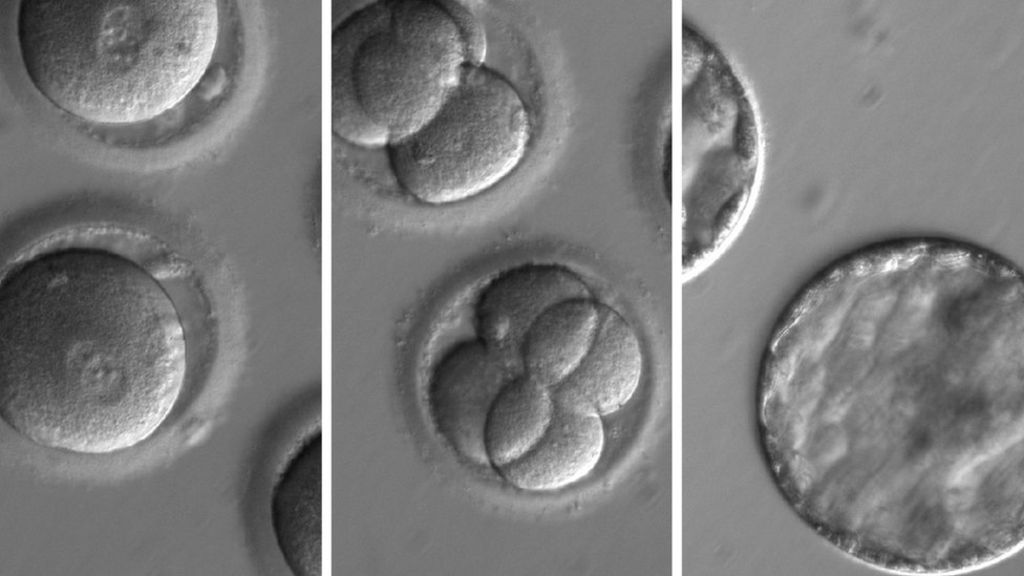 Cela ouvre potentiellement la porte à la prévention de 10.000 désordres transmis depuis des siècles. L’équipe américaine et sud-coréenne a permis aux embryons de se développer pendant cinq jours avant d’arrêter l’expérience.
Cela ouvre potentiellement la porte à la prévention de 10.000 désordres transmis depuis des siècles. L’équipe américaine et sud-coréenne a permis aux embryons de se développer pendant cinq jours avant d’arrêter l’expérience.
La science passe par un âge d’or grâce à une nouvelle technologie appelée Crispr. Ses applications en médecine sont vastes et comprennent l’idée d’éliminer les fautes génétiques qui causent des maladies de la fibrose kystique, au cancer du sein.
La cardiomyopathie hypertrophique : Les équipes américaines de l’Université de Santé et de Sciences de l’Oregon et l’Institut Salk ainsi que l’Institut pour la Science de Base en Corée du Sud se sont concentrés sur la cardiomyopathie hypertrophique.
Ce trouble fréquent, affecte une personne sur 500 et peut conduire à un arrêt cardiaque. Il est causé par une erreur dans un seul gène (une instruction dans l’ADN), et quiconque le porte a un risque accru de le transmettre à leurs enfants.
Dans l’étude, publiée dans la revue Nature, la réparation génétique s’est produite pendant la conception. Les spermatozoïdes d’un homme souffrant d’une cardiomyopathie hypertrophique ont été injectés dans des ovules saines avec la technologie Crispr pour corriger le défaut.
Cela ne fonctionnait pas tout le temps, mais 72% des embryons étaient exempts de mutations pathogènes.
Un avantage éternel : Le Docteur Shoukhrat Mitalipov, un membre de l’équipe de recherche, a déclaré : « En utilisant cette technique, il est possible de réduire le fardeau de cette maladie héréditaire sur la famille et éventuellement sur la population humaine ».
Il y a eu de multiples tentatives avant, y compris, en 2015, des équipes en Chine utilisant la technologie Crispr pour corriger les défauts qui entraînent des troubles sanguins. Mais ils ne pouvaient pas corriger toutes les cellules, de sorte que l’embryon était une «mosaïque» de cellules saines et malades.
Nicole Mowbray vit avec une cardiomyopathie hypertrophique et a un défibrillateur implanté dans au cas où son cœur s’arrêterait. Mais elle ne sait pas si elle envisagera la correction de gènes : « Je ne voudrais pas transmettre quelque chose qui va entraîner à mon enfant une vie limitée ou douloureuse ».
L’avis des spécialistes : Darren Griffin, professeur de génétique à l’Université de Kent, a déclaré : « Peut-être que la plus grande question, et probablement celle qui sera le plus débattue, est de savoir si nous devrions modifier physiquement les gènes d’un embryon de FIV ».
L’étude a déjà été évaluée par le Docteur David King, du groupe de campagne Human Genetics Alert, qui a décrit la recherche comme «irresponsable» et une « course pour le premier bébé génétiquement modifié ».
Docteur Yalda Jamshidi, un étudiant en médecine génomique à l’Université St George de Londres, a déclaré : « L’étude est la première à montrer une correction réussie et efficace d’une mutation pathogène dans des embryons humains de stade précoce. Alors que nous commençons tout juste à comprendre la complexité des maladies génétiques, la correction de gènes sera probablement acceptable lorsque ses avantages potentiels, tant pour les individus que pour la société en général, dépassent leurs risques ».